تعديلات مرتقبة لإصلاح قطاع الأدوية
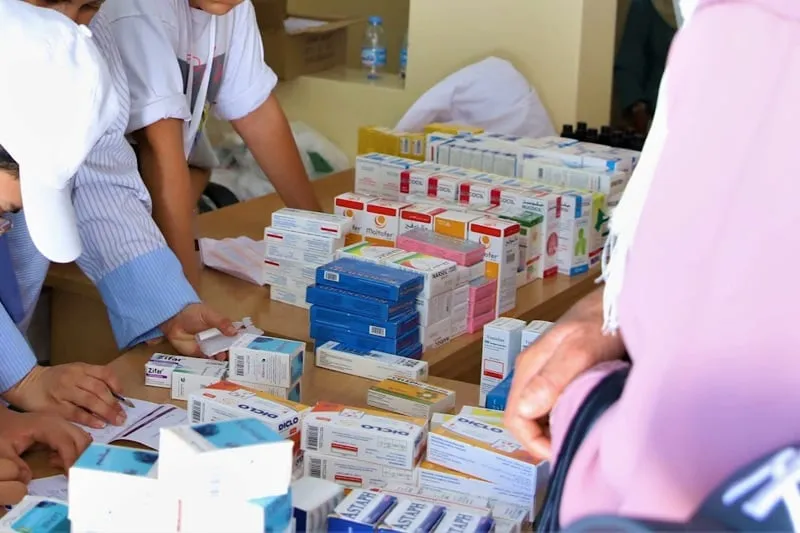
في إطار المسار الذي أطلقه المغرب لإصلاح المنظومة الصحية الوطنية فتحت الأمانة العامة للحكومة باب التعليق أمام العموم على مشروع قانون جديد طرحته وزارة الصحة والحماية الاجتماعية، يقضي بتغيير وتتميم القانون رقم 17.04 بمثابة مدونة الأدوية والصيدلة.
ويندرج مشروع هذا القانون، حسب مذكرته التقديمية، في إطار تنفيذ التعليمات الملكية الرامية إلى تحقيق السيادة الصحية والدوائية، إذ يهدف إلى “حصول المغرب على اعتماد منظمة الصحة العالمية، وإدراج الوكالة المغربية للأدوية والمنتجات الصحية في قائمة منظمة الصحة العالمية للهيئات التنظيمية ذات مستوى النضج الثالث والرابع”.
ويأتي هذا النص التشريعي الجديد في “سياق الجهود المتواصلة التي تبذلها المملكة المغربية من أجل تعزيز المنظومة الصحية الوطنية، والارتقاء بجودة وسلامة الأدوية والمنتجات الصحية، وملاءمة المنظومة الوطنية للأدوية مع المعايير المرجعية المعتمدة دولياً، ولا سيما تلك المتعلقة بدعم مهام الوكالة المغربية للأدوية والمنتجات الصحية وتعزيز أدوارها في مجالات الترخيص، ومراقبة السوق، والتفتيش، واليقظة الدوائية، بما يضمن حماية الصحة العامة وتحسين الولوج إلى الأدوية”.
ويهدف النص إلى تحيين وتدقيق بعض المقتضيات القانونية المتعلقة بتسويق الأدوية وشروط الترخيص لها، وتعزيز نظام اليقظة الدوائية وتكريس طابعه المؤسساتي والتنظيمي، إضافة إلى تقوية آليات مراقبة السوق وضمان جودة الأدوية بعد عرضها في السوق، وتوسيع نطاق اختصاصات التفتيش الصيدلي وتحسين نجاعته؛ كما يهدف إلى “ملاءمة الإطار القانوني مع متطلبات الحالات الاستثنائية، ولا سيما في حالة حدوث وباء أو حالة استعجال قصوى أو كارثة وطنية”.
وتشمل التغييرات التي يقترحها مشروع القانون سالف الذكر المادتين 7 و15 والفقرة الثانية من المادة 24، إضافة إلى المواد 120 و130 و131 و152، والفقرة الأولى من المادة 156، من القانون رقم 17.04 بمثابة مدونة الأدوية والصيدلة، الصادر بتنفيذه الظهير الشريف رقم 1.06.151 المؤرخ في الـ22 نونبر من عام 2006.
ونصت المادة الخامسة عشرة من المشروع، في باب الإذن بعرض الأدوية في السوق، على أنه يمكن للوكالة المغربية للأدوية والمنتجات الصحية أن تقرر سحب أو وقف هذا الإذن في حال عدم قيام صاحب الإذن بتسويق المنتج في السوق الوطنية أو تصديره داخل أجل يحدد بنص تنظيمي، مع إمكانية تمديد هذا الأجل بصفة استثنائية شريطة الإدلاء بمبررات.
وفي سياق متصل نصت الفقرة الثانية من المادة 24 التي يقترحها هذا المشروع على أنه “يتعين على المؤسسة الصيدلية الصناعية المصنعة لدواء بغرض تصديره أن تتوفر على مدخر احتياطي من الأدوية التي تقوم بصنعها أو استيرادها أو توزيعها، وذلك لضمان التموين العادي للسوق. وتطلب من الإدارة شهادة تثبت احترام المؤسسة قواعد حسن إنجاز الصنع المنصوص عليها في المادة 20 من هذا القانون”.
وجاء في مقتضيات المادة 120 وجوب إخبار الوكالة المغربية للأدوية والمنتجات الصحية، من طرف الصيدلي المسؤول بمؤسسة صيدلية المُشار إليه في المادة 74، بأي أثر جديد غير مرغوب فيه بلغ إلى علمه وكان ناتجا عن استعمال الأدوية، مع وجوب تعيين صيدلي مؤهل مكلف باليقظة الدوائية.
أما المادة 131 فتنص على تولي المراقبة من طرف صيادلة مفتشين محلفين طبقاً للتشريع المتعلق بأداء اليمين من طرف الأعوان محرري المحاضر، يفوضون بشكل قانوني لهذا الغرض من لدن مدير الوكالة المغربية للأدوية والمنتجات الصحية. فيما أقرت المادة 152 غرامات مالية تتراوح بين 100 ألف ومليون درهم على مخالفة أحكام المادة 24 سالفة الذكر.
كما نص مشروع القانون على “إحداث نظام وطني لليقظة الدوائية يضم مجموع المتدخلين في هذا المجال، وفقاً لقواعد الممارسات الجيدة لليقظة الدوائية المحددة من طرف الإدارة بعد استطلاع رأي المجلس الوطني للهيئة الوطنية للصيادلة”.
ووفقاً للوثيقة ذاتها تُتمم أحكام القانون سالف الذكر رقم 17.04 بالمادتين 8 مكرر و131 مكرر، وتنص الأولى على “إمكانية منح ترخيص بعرض دواء في السوق في إحدى الحالات التالية: إذا أظهرت المعطيات المتوفرة نسبة فائدة – مخاطر إيجابية أو مواتية لدواء يستجيب لحاجة طبية غير ملباة، شريطة التزام المؤسسة الصيدلية الصناعية صاحبة الطلب بتقديم المعطيات التكميلية اللازمة داخل أجل تحدده الوكالة المغربية للأدوية والمنتجات الصحية؛ أو في حالة وجود أسباب تتعلق بالصحة العامة، ولا سيما في حالة حدوث وباء أو حالة استعجال قصوى أو كارثة وطنية”.
The post تعديلات مرتقبة لإصلاح قطاع الأدوية appeared first on Hespress - هسبريس جريدة إلكترونية مغربية.